Formål
Overlevelsen af børnekræft er steget markant de seneste år – blandt andet grundet stamcelletransplantation, som anvendes ved højrisiko leukæmi.
Behandlingen kan dog medføre alvorlige og i nogle tilfælde livstruende bivirkninger samt risiko for senfølger. En stor del af de alvorlige bivirkninger skyldes skader på de små blodkar, der forsyner organerne med ilt (såkaldt endothel-toksicitet).
Disse bivirkninger kan i nogen grad imødegås med forebyggende behandling, men lægerne mangler metoder til at afgrænse den gruppe af børn, der kunne have gavn af dette.
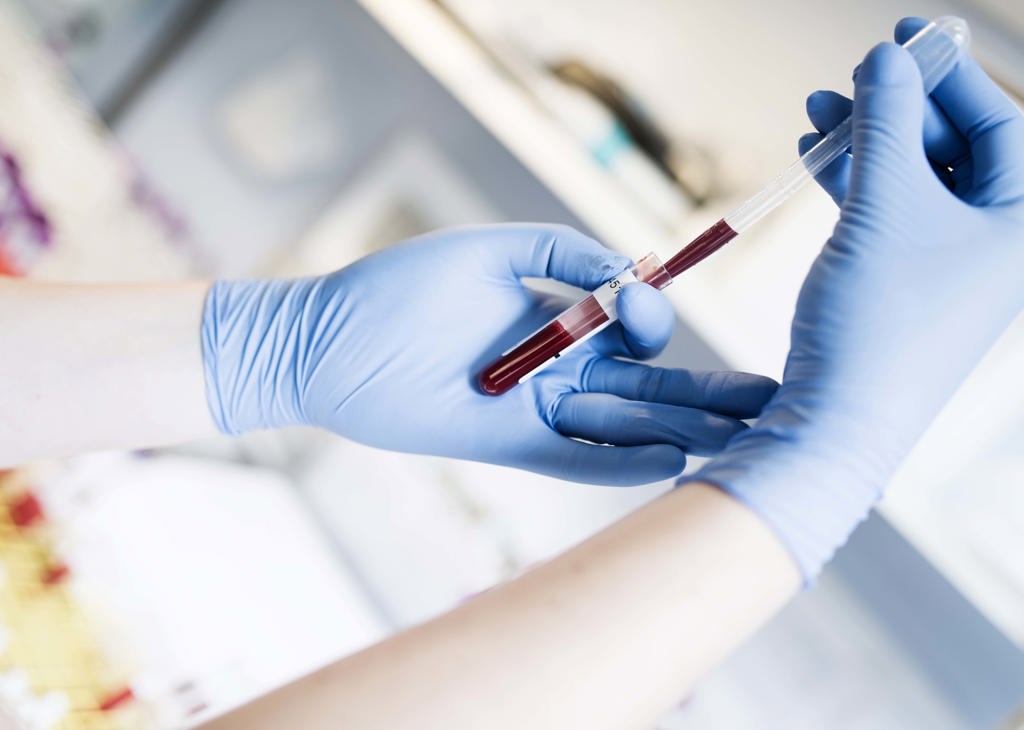
Formålet med ph.d.-studiet er at udvikle en blodprøve, der kan diagnosticere karskader tidligere og mere præcist samt identificere de børn, der er i risiko for at udvikle dem. Det sker ved at kombinere kliniske kriterier med kendte biomarkører og identificere nye biomarkører. Målet er at muliggøre tidligere og mere målrettet behandling.
Status
Projektet er i gang.
Delresultater
I studiet har forskerne undersøgt, hvordan behandlingsrelateret skade på blodkarrene påvirker risikoen for komplikationer efter transplantation, ved at måle niveauet af flere biomarkører som syndecan-1, solubel thrombomodulin (sTM) og solubel vascular endothelial growth receptor-1 (sVEGF-R1) i blodet. Biomarkørerne afspejler forskellige typer af skade på blodkarrene. Resultaterne viser, at børn der udvikler alvorlige leverkomplikationer eller svær akut graft-versus-host sygdom har forhøjede niveauer af disse biomarkører.
Foreløbige resultater tyder på, at disse biomarkører kan fungere som tidlige biomarkører for karskade og toksiske komplikationer. Disse markører vil kunne bidrage til tidligere diagnosticering og dermed give mulighed for hurtigere og mere målrettet behandling – med potentiale for at forbedre både overlevelse og livskvalitet hos børn, der gennemgår stamcelletransplantation.
Reference:
Horan DE, Weischendorff S, Johansson PI, Ifversen M, Nielsen CH, Müller K, Kielsen K. Syndecan-1 is Associated With Sinusoidal Obstruction Syndrome and Severe Acute Graft-Versus-Host Disease After Pediatric Hematopoietic Stem Cell Transplantation. Pediatr Blood Cancer. 2025 Oct;72(10):e31943. doi: 10.1002/pbc.31943. Epub 2025 Jul 25. PMID: 40880061. D.E. Horan, K. Kielsen, S. Weischendorff, M.E. Sørum, M. Kammersgaard, M. Ifversen, C.H. Nielsen, L. Ryde, P.I. Johansson, K. Müller. sVEGF-R1 in acute non-infectious toxicity syndromes after pediatric allogeneic hematopoietic stem cell transplantation. Transplant Immunology. 2024;82. Doi: 10.1016/j.trim.2023.101975. D.E. Horan, P.I. Johansson, M. Ifversen, C.H. Nielsen, K. Müller, K. Kielsen. Soluble Thrombomodulin Is Associated With Endothelial Dysfunction Syndromes After Pediatric Hematopoietic Stem Cell Transplantation. Pediatric Blood & Cancer. 2025:31675. Doi:10.1002/pbc.31675
Samarbejdspartnere
Projektet er finansieret i samarbejde med Team Rynkeby Fonden.
Støtteår
2021: 825.000 kr.
2023: 435.000 kr.